Подбор противоопухолевых препаратов
Химиотерапия — один из эффективных методов лечения онкологических заболеваний, основанный на применении фармакологических препаратов, оказывающих угнетающее действие на развитие опухолей. В зависимости от химической структуры и механизма действия выделяют несколько видов противоопухолевых лекарственных средств, назначение которых зависит от конкретной клинической ситуации и наличия в организме пациента характерных молекулярных маркеров.
Виды противоопухолевых препаратов
Существуют следующие виды противоопухолевой терапии:
- стандартная химиотерапия;
- таргетная;
- гормональная;
- иммунотерапия.
Стандартная химиотерапия
При подборе препаратов используются схемы стандартной химиотерапии, включающей цитостатики и противоопухолевые антибиотики.
Механизм действия различных цитостатиков может сильно отличаться, но суть сводится к угнетению процессов клеточного деления. Среди представителей данного класса соединений можно выделить 5-фторурацил, оксалиплатин, гемцитабин, винорелбин.
К противоопухолевым антибиотикам относятся соединения антрациклинового ряда, среди которых наиболее распространены блеомицин, доксорубицин, даунорубицин, эпирубицин, дактиномицин и митомицин. Препараты данной группы оказывают действие за счет ингибирования (замедления) синтеза ДНК и РНК посредством связывания с липидами клеточных мембран, а также изменения первичной и вторичной структуры нуклеиновых кислот.
Таргетная терапия
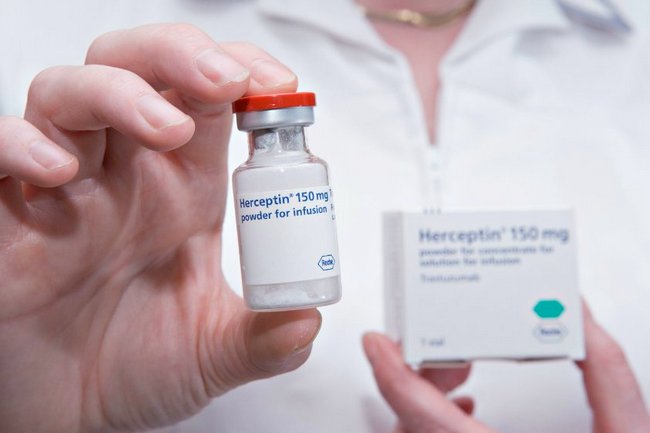
Таргетная (биологическая) терапия — это относительно новое направление в лекарственном лечении злокачественных опухолей. Суть сводится к блокированию действия конкретных целевых молекул, необходимых для прогрессирования опухоли. В отличие от стандартной химиотерапии, которая препятствует размножению всех активно пролиферирующих (делящихся) клеток в организме, таргетные препараты оказывают избирательное действие на какую-либо конкретную мишень (обычно белок), присутствующую в опухолевых клетках. Поиск таких мишеней в раковых клетках обязателен при подборе противоопухолевых препаратов. В результате удается достичь более выраженного терапевтического эффекта и минимизировать побочные эффекты.
Несмотря на существующие достоинства таргетных препаратов, они показаны пациентам только при наличии конкретных генетических маркеров. Так, например, препарат «Гливек» (Gleevec) оказывает действие при хроническом миелолейкозе, для которого в результате транслокации между 9-й и 22-й парой хромосом характерно образование химерного белка BCR-ABL. Моноклональное антитело «Герцептин» («Трастузумаб») оказывает эффект при наличии гиперэкспрессии гена Her-2/neu в опухолевой ткани. «Кризотиниб» показан при дефектах в генах ALK и ROS1. «Эрбитукс» — при отсутствии мутаций в гене K-ras.
Гормональная терапия

Суть гормональной противоопухолевой терапии сводится к восстановлению регуляции некоторых функций клеток. Кроме того, возможна стимуляция дифференцировки и цитостатический эффект. Такие препараты находят применение при лечении гормонозависимых опухолей при раке молочной железы, простаты, эндометрия, меланомы и др.
Подбор противоопухолевых препаратов может дополняться следующими типами гормональных средств:
- андрогены. Чаще используются тестостерон, метилтестостерон, пролотестон;
- эстрогены. Наиболее распространены гестонорона капроат, мегестрол и др.;
- антагонисты эстрогенов. Самый известный представитель данной группы — «Тамоксифен»;
- антагонисты андрогенов. Представители данной группы препаратов: «Бикалутамид», «Флутамид»;
- глюкокортикоиды. Наиболее известны «Преднизолон», «Дексаметазон»;
- ингибиторы ароматазы. Представителями данной группы являются «Анастрозол», «Летрозол».
Иммунотерапия
Одним из самых новых и перспективных методов борьбы со злокачественными новообразованиями является иммунотерапия. Её суть — активизировать силы иммунной системы пациента и заставить их противостоять опухолевым клеткам. В качестве препаратов используются вакцины, интерфероны, колониестимулирующие факторы, моноклональные антитела, интерлейкины и др.
Иммунотерапия может проводиться как с целью уничтожения опухоли, так и для уменьшения побочных эффектов от химиопрепаратов, предупреждения осложнений и предотвращения прогрессирования заболевания. Среди используемых препаратов можно отметить «Ниволумаб», «Бевацизумаб», «Пембролизумаб», «Ипилимумаб».
Система оценки ответа на химиотерапию
Для оценки эффективности проводимой противоопухолевой терапии рекомендовано использовать международную систему критериев.
- Полный ответ. Опухоль не выявлена. Полная регрессия.
- Частичный ответ. Опухоль регрессировала на 50 % и более. Новые очаги поражения не выявлены.
- Минимальный ответ. Опухоль регрессировала на 25–50 %.
- Стабилизация. Объем опухоли не изменился либо уменьшился менее чем на 25 %. Новые очаги поражения не выявлены.
- Прогрессирование заболевания. Объем первичной опухоли увеличился, появились новые очаги на фоне проводимого лечения.
Существуют злокачественные опухоли, которые заведомо резистентны к лекарственной терапии, а потому к ним применяются другие методы лечения. Резистентность опухолевых клеток бывает первичная, то есть возникшая спонтанно, и вторичная, которая возникает на фоне химиотерапии и зачастую является единственным препятствием к полному излечению заболевания при помощи одного химиопрепарата.
Побочные эффекты противоопухолевых препаратов
Любая злокачественная опухоль является такой же частью организма, как и здоровая ткань. Современные препараты не способны влиять исключительно на злокачественные клетки. Они оказывают свое влияние, в том числе и на здоровые клетки организма, чем и вызвано развитие побочных эффектов:
- угнетение кроветворной функции. Это одно из самых частых осложнений, которое может усиливаться с увеличением дозы, при добавлении лучевой терапии, а также при использовании сложных химиотерапевтических схем, включающих несколько препаратов. Депрессия гемопоэза сопряжена с угрозой для жизни, поскольку лишает организм возможности противостоять любой инфекции. При проведении химиотерапии контролируют показатели общего анализа крови, в первую очередь количество лейкоцитов;
- снижение аппетита, тошнота и рвота, запор, диарея;
- алопеция (облысение). Происходит из-за повреждения волосяных луковиц. После отмены препарата рост волос возобновляется;
- различные препараты могут обладать кардио-, гепато-, нефро-, нейротоксичностью;
- у пациентов может развиваться слабость, депрессия, повреждение слизистых и кожных покровов.
Персонализированный подбор противоопухолевых препаратов
К сожалению, на сегодняшний день подбор большинства противоопухолевых препаратов происходит исключительно опытным путем. Доктор учитывает гистологию и локализацию опухоли, степень её распространенности и дифференцировки. Однако при схожих клинических характеристиках ответ на проводимое лечение может отличаться. Выживаемость варьируется от нескольких месяцев до нескольких лет. Всё это указывает на значительную молекулярную и генетическую неоднородность опухоли. Ученые едины во мнении, что именно молекулярные особенности опухоли определяют её чувствительность к той или иной схеме химиотерапии.
Так, например, чувствительность к фторпиримидинам определяется наличием либо отсутствием мутаций в гене DPD, для чего выполняют его секвенирование. «Иринотекан» назначают с учетом мутационного статуса гена UGT1A1, который определяется при помощи метода полимеразной цепной реакции.
Препараты «Эрлотиниб», «Гефитиниб», «Афатиниб» назначают лишь при наличии активирующих мутаций в гене EGFR в ткани немелкоклеточного рака легкого. В то же время мутация T790M в указанном гене является маркером резистентности опухоли к ингибиторам EGFR.
Препараты «Цетуксимаб» и «Панитумумаб» назначают при раке легкого, толстой и прямой кишки, а также при поражении поджелудочной железы. Показанием к назначению является отсутствие мутаций в гене KRAS, которые могут быть выявлены при помощи полимеразной цепной реакции в режиме реального времени.
«Ниволумаб» и «Пембролизумаб» назначаются при меланоме и немелкоклеточном раке легкого только при наличии экспрессии в опухолевой ткани белка PD-L1. Исследование выполняется иммуногистохимическим методом с использованием моноклональных антител.
Персонализированный подход к лечению — это новое приоритетное направление в онкологии, которое стремительно развивается и приходит на смену эмпирическому назначению химиотерапии. Всё идет к тому, что подбор противоопухолевых препаратов должен быть обусловлен наличием в опухолевых клетках определенных мишеней. В таком случае лечение будет строго избирательным и позволит достигать максимального результата при минимуме побочных эффектов.

 В нашем медцентре
В нашем медцентре  Онлайн (по телефону, Skype, Whatsapp, Viber, Telegram)
Онлайн (по телефону, Skype, Whatsapp, Viber, Telegram)