16 Декабря 2019г.
16 Декабря 2019г.
Хромосомные болезни
Организм человека является сложной системой, деятельность которой регулируется на различных уровнях. При этом определенные вещества должны участвовать в конкретных биохимических процессах, чтобы все клетки, органы и целые системы могли правильно функционировать. А для этого требуется заложить правильное основание. Подобно тому, как многоэтажный дом не выстоит без соответствующим образом подготовленного фундамента, «здание» человеческого тела требует корректной передачи наследственного материала. Именно заложенный в нем генетический код управляет развитием зародыша, позволяет сформироваться всем взаимодействиям и обуславливает нормальное существование человека.
Однако в некоторых случаях в наследственной информации появляются ошибки. Они могут возникать на уровне отдельных генов или же касаться их крупных объединений. Подобные изменения называются генными мутациями. В отдельных ситуациях проблема относится к целым хромосомам, то есть к структурным единицам клетки. Соответственно, их называют хромосомными мутациями. Наследственные болезни, развивающиеся вследствие нарушений хромосомного набора или строения хромосом, получили название хромосомных.
В норме каждая клетка организма содержит одно и то же количество хромосом, объединенных в пары с одинаковыми генами. У человека полный набор состоит из 23 пар, и только в половых клетках вместо 46 хромосом находится половинное число. Это необходимо для того, чтобы в процессе оплодотворения при слиянии сперматозоида и яйцеклетки получилась полноценная комбинация со всеми необходимыми генами. Гены распределены по хромосомам не случайно, а в строго определенном порядке. При этом линейная последовательность сохраняется одинаковой для всех людей.
Однако в процессе образования половых клеток могут произойти различные «ошибки». В результате мутаций изменяется количество хромосом или их структура. По этой причине после оплодотворения в яйцеклетке может оказаться избыточное или, напротив, недостаточное количество хромосомного материала. Из-за дисбаланса процесс развития зародыша нарушается, что может привести к самопроизвольному прерыванию беременности, рождению мертвого ребенка либо развитию наследственного хромосомного заболевания.
Этиология хромосомных заболеваний
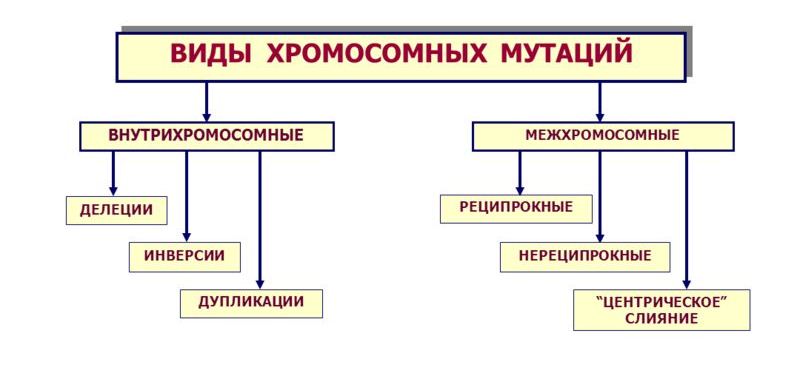
К этиологическим факторам хромосомных патологий относятся все разновидности хромосомных мутаций. Кроме того, некоторые геномные мутации также способны оказывать подобное действие.
У человека встречаются делеции, дупликации, транслокации и инверсии, то есть все типы мутаций. При делеции и дупликации генетическая информация оказывается в недостаточном и избыточном количестве соответственно. Поскольку современными методами можно выявить отсутствие даже небольшой части генетического материала (на уровне гена), то провести четкую границу между генными и хромосомными заболеваниями практически невозможно.
Транслокации представляют собой обмен генетическим материалом, который происходит между отдельными хромосомами. Иными словами, происходит перемещение участка генетической последовательности на негомологичную хромосому. Среди транслокаций выделяют две важные группы – реципрокные и Робертсоновские.
Транслокации реципрокного характера без потери задействованных участков называются сбалансированными. Они, как и инверсии, не вызывают потери генной информации, поэтому не приводят к паталогическим эффектам. Тем не менее, при дальнейшем участии таких хромосом в процессе кроссинговера и редукции могут образовываться гаметы с несбалансированными наборами, обладающие недостаточным набором генов. Их участие в процессе оплодотворения приводит к тому, что у потомства развиваются те или иные наследственные синдромы.
Для Робертсоновских транслокаций характерно участие двух акроцентрических хромосом. В ходе процесса короткие плечи утрачиваются, а длинные сохраняются. Из 2 исходных хромосом формируется одна цельная, метацентрическая. Несмотря на потерю части генетического материала развития патологий в таком случае обычно не происходит, поскольку функции утраченных участков компенсируются аналогичными генами в остальных 8 акроцентрических хромосомах.
При концевых делециях (то есть при их утрате) может сформироваться кольцевая хромосома. У ее носителя, получившего такой генный материал от одного из родителей, отмечают частичную моносомию по концевым участкам. При разрыве через центромеру может сформироваться изохромосома, имеющая одинаковые по набору генов плечи (у обычной хромосомы они отличаются).
В некоторых случаях может развиваться однородительская дисомия. Она возникает, если при нерасхождении хромосом и оплодотворении возникнет трисомия, а после этого одна из трех хромосом будет удалена. Механизм этого явления в настоящее время не изучен. Однако в результате в хромосомном наборе появится две копии хромосомы одного родителя, в то время как часть генной информации от второго родителя будет утеряна.
Многообразие вариантов искажения хромосомного набора обуславливает различные формы заболеваний.
Классификация хромосомных патологий
Имеется три базовых принципа, которые позволяют точно классифицировать возникшую хромосомную патологию. Их соблюдение обеспечивает однозначное указание на форму отклонения.
Согласно первому принципу необходимо определить характеристику мутации, генной или хромосомной, причем требуется также четко указать конкретную хромосому. К примеру, это может быть простая трисомия по 21 хромосоме или триплоидия. Сочетание индивидуальной хромосомы и типа мутации определяет формы хромосомной патологии. Благодаря соблюдению этого принципа можно точно установить, в какой структурной единице имеются изменения, а также выяснить, зафиксирован избыток или недостаток хромосомного материала. Такой подход более эффективен, чем классификация по клиническим признакам, поскольку многие отклонения вызывают сходные нарушения развития организма.
Согласно второму принципу нужно определить тип клеток, в котором произошла мутация – зигота или гамета. Мутации в гаметах приводят к появлению полных форм хромосомного заболевания. В каждой клетке организма будет содержаться копия генетического материала с хромосомной аномалией. Если же нарушение происходит позднее, на этапе зиготы или во время дробления, то мутация классифицируется как соматическая. В этом случае часть клеток получает изначальный генетический материал, а часть – с измененным хромосомным набором. Одновременно в организме может присутствовать два и более типа наборов. Их сочетание напоминает мозаику, поэтому такая форма болезни называется мозаичной. Если в организме присутствует более 10% клеток с измененным хромосомным набором, клиническая картина повторяет полную форму.
Согласно третьему принципу выявляется поколение, в котором мутация появилась первый раз. Если изменение было отмечено в гаметах здоровых родителей, то говорят о спорадическом случае. Если же оно уже имелось в материнском или отцовском организме, то речь идет о наследуемой форме. Значительная часть унаследованных хромосомных заболеваний вызывается робертсоновскими транслокациями, инверсиями и сбалансированными реципрокными транслокациями. В процессе мейоза они могут привести к образованию патологической комбинации.
Полная точная диагностика подразумевает, что установлены тип мутации, затронутая хромосома, выяснен полный или мозаичный характер заболевания, а также установлена передача по наследству или спорадическое возникновение. Получить необходимые для этого данные можно при проведении генетической диагностики с использованием проб пациента, а в некоторых случаях и его родственников.
Общие вопросы
Интенсивное развитие генетики в течение последних десятилетий позволило развить отдельное направление хромосомной патологии, которая постепенно приобретает все большое значение. К этой области относятся не только хромосомные болезни, но и различные нарушения во время внутриутробного развития (к примеру, выкидыши). В настоящее время счет аномалий идет уже на 1000. Свыше ста форм характеризуются клинически очерченной картиной и называются синдромами.
Выделяется несколько групп болезней. Триплоидией называется случай, при котором в клетках организма имеется лишняя копия генома. Если же появился дубликат только одной хромосомы, то подобное заболевание называется трисомией. Также причинами аномального развития организма могут быть делеции (удаленные участки генетического кода), дупликации (соответственно, лишние копии генов или их групп) и иные дефекты. Английский врач Л. Даун в 1866 году описал одну из самых известных болезней такого рода. Синдром, получивший его имя, развивается при наличии лишней копии 21 хромосомы (трисомия-21). Трисомии по другим хромосомам, как правило, заканчиваются выкидышами или приводят к смерти в детском возрасте из-за серьезных нарушений в развитии.
Позже были открыты случаи моносомии по X-хромосоме. В 1925 году Шерешевский Н.А и в 1938 году Тернер Г. описали его симптомы. Трисомия-XXY, которая встречается у мужчин, была описана Клайнфельтером в 1942 году.
Указанные случаи заболеваний стали первыми объектами исследований в этой области. После того, как расшифровали этиологию трех перечисленных синдромов, фактически появилось направление хромосомных болезней. В течение 60-х годов дальнейшие цитогенетические исследования привели к формированию клинической цитогенетики. Ученые доказали связь между патологическими отклонениями и хромосомными мутациями, а также получили статистические данные о частоте появления мутаций у новорожденных и в случаях самопроизвольного прерывания беременности.
Типы хромосомных аномалий
Хромосомные аномалии могут быть как относительно крупными, так и небольшими. В зависимости от их размеров меняются методы исследования. К примеру, для точечных мутаций, делеций и дупликаций, касающихся участков длиной в сотню нуклеотидов, обнаружение при помощи микроскопа невозможно. Определить хромосомное нарушение при помощи метода дифференциального окрашивания возможно только в том случае, если величина затронутого участка исчисляется в миллионах нуклеотидов. Небольшие мутации можно выявить лишь при помощи установления нуклеотидной последовательности. Как правило, большие по размерам нарушения (к примеру, видимые в микроскоп) приводят к более выраженному воздействию на функционирование организма. Кроме того, аномалия может затрагивать не только ген, но и участок наследственного материала, функции которого в настоящее время не исследованы.
Моносомией называется аномалия, выражающаяся в отсутствии одной из хромосом. Обратным случаем является трисомия – добавление лишней копии хромосомы к стандартному набору из 23 пар. Соответственно, меняется и число копий генов, которые в норме присутствуют в двух экземплярах. При моносомии отмечается нехватка гена, при трисомии – его избыток. Если хромосомная аномалия приводит к изменению числа отдельных участков, то говорят о частичной трисомии или моносомии (к примеру, по плечу 13q).
Известны также случаи однородительской дисомии. При этом пара гомологичных хромосом (либо одна и часть гомологичной ей) попадает в организм от одного из родителей. Причиной является неизученный механизм, предположительно состоящий из двух фаз – образование трисомии и удаление одной из трех хромосом. Воздействие однородительской дисомии может быть как незначительным, там и заметным. Дело в том, что если в одинаковых хромосомах имеется рецессивный мутантный аллель, то он автоматически проявляется. В то же время родитель, от которого была получена хромосома с мутацией, из-за гетерозиготности по гену может не иметь проблем со здоровьем.
Из-за высокой важности генетического материала для всех этапов развития организма даже небольшие аномалии могут вызвать серьезные изменения в скоординированной деятельности генов. Ведь их совместная работа шлифовалась в течение миллионов лет эволюции. Неудивительно, что последствия от возникновения такой мутации, скорее всего, начинают проявляться уже на уровне гамет. Особенно сильно они влияют на мужчин, поскольку зародыш в определенный момент должен перейти с женского пути развития на мужской. Если же активности соответствующих генов недостаточно, возникают различные отклонения, вплоть до гермафродитизма.
Исследование хромосомных отклонений
Первые исследования эффектов от хромосомных нарушений стали проводить в 60-х годах, после того как был установлен хромосомный характер некоторых заболеваний. Можно условно выделить две большие группы связанных эффектов: врожденные пороки развития и изменения, вызывающие летальные исходы. Современная наука располагает сведениями, что хромосомные аномалии начинают проявляться уже на стадии зиготы. Летальные эффекты при этом являются одной из основных причин гибели плода в утробе (этот показатель у человека достаточно высок).
Хромосомные аберрации – это изменение структуры хромосомного материала. Они могут как возникать спорадически, так и передаваться по наследству. Точная причина, по которой они появляются, не установлена. Ученые полагают, что за некоторую часть таких мутаций отвечают различные факторы окружающей среды (например, химически активные вещества), которые воздействуют на эмбрион или даже на зиготу. Интересен тот факт, что большая часть хромосомных аберраций обычно связана с хромосомами, которые зародыш получает от отца.
Значительная часть хромосомных аберраций встречается очень редко и была обнаружена один раз. В то же время некоторые другие достаточно часто встречаются, причем даже у людей, не связанных родственными узами. К примеру, широко распространена транслокация центромерных или близких к ним районов 13 и 14 хромосом. Утрата неактивного хроматина коротких плеч практически не влияет на состояние здоровья. При аналогичных робертсоновских транслокациях в кариотип попадает 45 хромосом.
Примерно две трети всех обнаруживаемых у новорожденных хромосомных аномалий компенсируются за счет других копий генов. По этой причине они не несут серьезной угрозы нормальному развитию ребенка. Если же компенсация нарушения невозможна, возникают пороки развития. Часто такая несбалансированная аномалия выявляется у больных с умственной отсталостью и другими врожденными пороками, а также у плода после самопроизвольных абортов.
Известны компенсированные аномалии, которые способны наследоваться из поколения в поколение без возникновения заболеваний. В некоторых случаях такая аномалия может перейти в несбалансированную форму. Так, если имеется транслокация, затрагивающая 21 хромосому, возрастает риск трисомии по ней. По статистике такие транслокации имеются у каждого 20 ребенка, у которого зафиксирована трисомия-21, причем в каждом пятом случае аналогичное нарушение есть у одного из родителей. Поскольку большая часть детей с вызванной транслокацией трисомией-21 рождается у молодых (менее 30 лет) мам, то в случае обнаружения этого заболевания у ребенка необходимо произвести диагностическое обследование молодых родителей.
Риск появления нарушений, которые не компенсируются, сильно зависит от транслокации, поэтому теоретические расчеты затруднены. Тем не менее, приблизительно определить вероятность соответствующей патологии можно на основании статистических данных. Такая информация собрана для распространенных транслокаций. В частности, робертсоновская транслокация между 14 и 21 хромосомами у матери с вероятностью 2 процента приводит к трисомии-21 у ребенка. Эта же транслокация у отца передается по наследству с вероятностью 10%.
Распространенность хромосомных аномалий
Результаты исследований показывают, что как минимум десятая часть яйцеклеток после оплодотворения и около 5-6 процентов плодов имеют различные хромосомные аномалии. Как правило, на 8-11 неделе в таком случае происходит самопроизвольное прерывание беременности. В некоторых случаях они вызывают более поздние выкидыши или приводят к рождению мертвого ребенка.
У новорожденных (по результатам обследования более 65 тысяч детей) изменение числа хромосом либо значительные хромосомные аберрации встречаются примерно у 0,5% от общего количества. Как минимум каждый 700-й имеет трисомию по 13, 18 или 21 хромосоме; около 1 из 350 мальчиков имеют расширенный до 47 единиц набор хромосом (кариотипы 47,XYY и 47,XXY). Моносомия по X-хромосоме встречается реже – единичные случаи на несколько тысяч. Порядка 0,2% имеют компенсированные хромосомные аберрации.
У взрослых иногда также выявляются наследуемые отклонения (как правило, компенсированные), иногда с трисомией по половым хромосомам. Исследования также показывают, что примерно 10-15 процентов от общего числа случаев умственной отсталости могут быть объяснены наличием хромосомной аномалии. Этот показатель значительно возрастает, если вместе с нарушениями умственного развития наблюдаются анатомические дефекты. Бесплодие также часто вызывается лишней половой хромосомой (у мужчин) и моносомией/аберрацией по X хромосоме (у женщин).
Связь хромосомных аномалий и злокачественных образований
Как правило, исследование клеток злокачественных новообразований приводит к обнаружению видимых в микроскоп хромосомных аномалий. Сходные результаты дает проверка при лейкозе, лимфоме и ряде других заболеваний.
В частности, для лимфом нередким случаем является обнаружение транслокации, сопровождающейся разрывом внутри или рядом с локусом тяжелой цепи иммуноглобулина (14 хромосома). При этом ген MYC перемещается с 8 хромосомы на 14.
Для миелолейкоза в большинстве случаев (свыше 95%) фиксируется транслокация между 22 и 9 хромосомами, вызывающая появление характерной «филадельфийской» хромосомы.
Бластный криз в процессе развития сопровождается появлением в кариотипе последовательных хромосомных аномалий.
Методами дифференциального окрашивания с последующим наблюдением в микроскоп, а также при помощи молекулярно-генетических способов тестирования, можно своевременно выявлять хромосомные аномалии при различных лейкозах. Эта информация помогает сделать прогноз развития, по ней уточняется диагноз и корректируется терапия.
Для распространенных солидных опухолей, таких, как рак толстой кишки, рак молочной железы и т.д. обычные цитогенетические методы применимы с некоторыми ограничениям. Тем не менее, характерные для них хромосомные аномалии также были выявлены. Имеющиеся в опухолях отклонения часто связаны с генами, отвечающими за процесс нормального роста клеток. Из-за амплификации (образования множественных копий) гена иногда отмечается формирование мелких мини-хромосом в клетках новообразований.
В некоторых случаях появление злокачественного образования вызывает потеря гена, который должен обеспечивать подавление пролиферации. Причин может быть несколько: делеции и разрыв в процессе транслокации являются наиболее частыми. Мутации такого рода принято считать рецессивными, поскольку наличие даже одной нормальной аллели обычно обеспечивает достаточный контроль роста. Нарушения могут появляться или наследоваться. Если же в геноме отсутствует нормальная копия гена, то пролиферация перестает зависеть от регулирующих факторов.
Таким образом, наиболее значимыми хромосомными аномалиями, влияющими на возникновение и рост злокачественных новообразований, являются следующие типы:
- транслокации, поскольку они могут привести к нарушению нормального функционирования генов, отвечающих за пролиферацию (либо вызвать их усиленную работу);
- делеции, которые наряду с прочими рецессивными мутациями вызывают изменения в процессе регуляции роста клетки;
- рецессивные мутации, из-за рекомбинации становящиеся гомозиготными и оттого проявляющиеся в полной мере;
- амплификации, стимулирующие пролиферацию клеток опухоли.
Выявление указанных мутаций в ходе генетической диагностики может указывать на повышенный риск развития злокачественных новообразований.
Известные заболевания хромосомной природы
Одним из самых известных заболеваний, происходящих по причине наличия аномалий в генетическом материале, является синдром Дауна. Он обуславливается трисомией по 21 хромосоме. Характерным признаком этой болезни является отставание в развитии. Дети испытывают серьезные проблемы во время обучения в школе, часто им требуется альтернативная методика преподавания материала. Вместе с тем отмечаются нарушения физического развития – плоское лицо, увеличенные глаза, клинодактилия и другие. Если такие люди прикладывают значительные усилия, они могут достаточно хорошо социализироваться, известен даже случай успешного получения высшего образования мужчиной с синдромом Дауна. У больных повышен риск заболеть деменцией. Это и ряд других причин приводит к небольшой продолжительности жизни.
К трисомии относится и синдром Патау, только в этом случае имеется три копии 13 хромосомы. Для заболевания характерны множественные пороки развития, часто с полидактилией. В большинстве случаев отмечается нарушение деятельности центральной нервной системы либо ее неразвитость. Часто (примерно в 80 процентах) больные имеют пороки развития сердца. Тяжелые нарушения приводят к высокой смертности – в первый год жизни умирает до 95% детей с этим диагнозом. Заболевание не поддается лечению или коррекции, как правило, можно лишь обеспечить достаточно постоянный контроль состояния человека.
Еще одна форма трисомии, с которой рождаются дети, относится к 18 хромосоме. Заболевание в этом случае носит название синдрома Эдвардса и характеризуется множественными нарушениями. Деформируются кости, часто наблюдается измененная форма черепа. Сердечно-сосудистая система обычно с пороками развития, также проблемы отмечаются с органами дыхания. В результате около 60% детей не доживают до 3 месяцев, к 1 году умирает до 95% детей с этим диагнозом.
Трисомия по другим хромосомам у новорожденных практически не встречается, поскольку почти всегда приводит к преждевременному прерыванию беременности. В части случаев рождается мертвый ребенок.
С нарушениями числа половых хромосом связан синдром Шерешевского-Тернера. Из-за нарушений в процессе расхождения хромосом теряется X-хромосома в женском организме. В результате организм не получает должного количества гормонов, поэтому нарушается его развитие. В первую очередь это относится к половым органам, которые развиваются лишь отчасти. Практически всегда для женщины это обозначает невозможность иметь детей.
У мужчин полисомия по Y или X хромосоме приводит к развитию синдрома Клайнфельтера. Для этого заболевания характерна слабая выраженность мужских признаков. Зачастую сопровождается гинекомастией, возможно отставание в развитии. В большинстве случаев наблюдаются ранние проблемы с потенцией и бесплодие. В этом случае, как и для синдрома Шерешевского-Тернера, выходом может стать экстракорпоральное оплодотворение.
Благодаря методам пренатальной диагностики стало возможным выявление этих и других заболеваний у плода во время беременности. Семейные пары могут принять решение о прерывании беременности, чтобы попробовать зачать другого ребенка. Если же они принимают решение выносить и родить малыша, то знание особенностей его генетического материала позволяет заранее подготовиться к определенным методам профилактики или лечения.
Анализ кариотипа
Кариотип – систематизированный набор хромосом ядра клетки с его количественными и качественными характеристиками.

Нормальный женский кариотип - 46,XX | Нормальный мужской кариотип - 46,XY
Исследование кариотипа - процедура, призванная выявить отклонения структуры строения и числа хромосом.
Показания для кариотипирования:
- Множественные врожденные пороки развития, сопровождаемые клинически анормальным фенотипом или дизморфизмом
- Умственная отсталость или отставание в развитии
- Нарушение половой дифференцировки или аномалии полового развития
- Первичная или вторичная аменорея
- Аномалии спермограммы – азооспермия или тяжелая олигоспермия
- Бесплодие неясной этиологии
- Привычное невынашивание
- Родители пациента со структурными хромосомными аномалиями
- Повторное рождение детей с хромосомными аномалиями
К сожалению, с помощью исследования кариотипа можно определить лишь крупные структурные перестройки. В большинстве же случаев аномалии строения хромосом представляют собой микроделеции и микродупликации невидимые под микроскопом. Однако такие изменения хорошо идентифицируются современными молекулярными цитогенетическими методами - флуоресцентной гибридизацией (FISH) и хромосомным микроматричным анализом.
Флуоресцентная гибридизация in situ (FISH)
Аббревиатура FISH расшифровывается как fluorescent in situ hybridization – флуоресцентная гибридизация на месте. Это цитогенетический метод, который применяют для выявления и определения положения специфической последовательности ДНК на хромосомах. Для этого используют специальные зонды - нуклеозиды, соединенные с флуорофорами или некоторыми другими метками. Визуализацию связавшихся ДНК-зондов проводят при помощи флуоресцентного микроскопа.
Метод FISH позволяет изучать небольшие хромосомные перестройки, которые не идентифицируются при стандартном исследовании кариотипа. Однако, имеет один существенный недостаток. Зонды являются специфичными только к одному участку генома и, как следствие, при одном исследовании можно определить наличие или число копий только этого участка (или нескольких при использовании многоцветных зондов). Поэтому важным является правильная клиническая предпосылка, а FISH анализ может только подтвердить иди не подтвердить диагноз.
Альтернативой этому методу является хромосомный микроматричный анализ, который при такой же точности, чувствительности и специфичности определяет количество генетического материала в сотнях тысяч (и даже миллионах) точек генома, что дает возможность диагностики практически всех известных микроделеционных и микродупликационных сииндромов.
Хромосомный микроматричный анализ

Хромосомный микроматричный анализ – молекулярно-цитогенетический метод для выявления вариаций числа копий ДНК по сравнению с контрольным образцом. При выполнении этого анализа исследу¬ются все клинически значимые участки генома, что позволяет с максимальной точностью исключить хромосомную патологию у обследуемого. Таким образом могут быть выявлены патогенные деле¬ции (исчезновение участков хромосом), дупликации (появление дополни¬тельных копий генетического материала), участки с потерей гетерозиготности, которые имеют важное значение при болезнях импринтинга, близкородственных браках, аутосомно-рецессивных заболеваниях.
Когда необходим хромосомный микроматричный анализ
- В качестве теста первой линии для диагностики пациентов с дизморфиями, врожденными пороками развития, умственной отсталостью/задержкой развития, множественными врожденными аномалиями, аутизмом, судорогами или любым подозрением на наличие геномного дисбаланса.
- В качестве замены кариотипа, FISH и сравнительной геномной гибридизации, если подозревается микроделеционный/микродупликационный синдром.
- В качестве исследования для выявления несбалансированных хромосомных аберраций.
- В качестве дополнительного диагностического исследования при моногенных заболеваниях, связанных с функциональной потерей одного аллеля (гаплонедостаточностью), особенно если при секвенировании не удается выявить патогенную мутацию, и делеция всего гена может быть причиной.
- Для определения происхождения генетического материала при однородительских дисомиях, дупликациях, делециях.
Нажимая на кнопку, вы даете согласие на обработку персональных данных